Das BMBF-Projekt e:Kid hat Computermodelle entwickelt, die eine personalisierte Immunsuppression nach der Transplantation ermöglichen. Sie sollen die Überlebenszeiten der Spenderorgane verlängern und die Lebensqualität Betroffener verbessern.
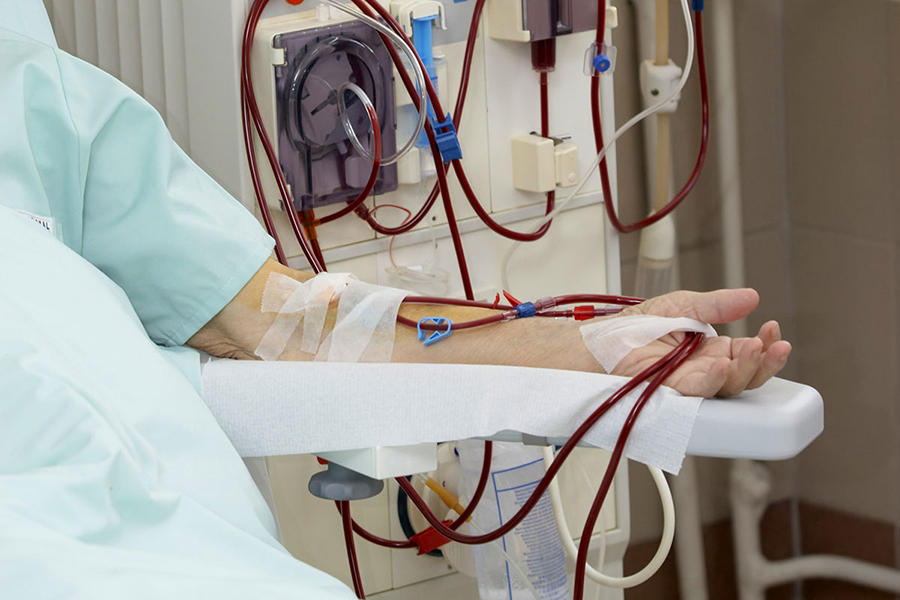
Während sie auf ein Spenderorgan warten, sind die Patientinnen und Patienten auf die Dialyse angewiesen.
Zeljko Bozic/Thinkstock
Etwa 9.500 Menschen stehen in Deutschland auf der Warteliste für ein Spenderorgan. 7.500 davon warten auf eine Nierentransplantation – die aktuelle Therapie der Wahl bei Nierenversagen. Diese Erkrankung kann sich beispielsweise als Folge von Diabetes mellitus oder Bluthochdruck entwickeln. „Die Zahl nierenkranker Patientinnen und Patienten nimmt in Deutschland immer weiter zu“, weiß Prof. Dr. Nina Babel. Die Medizinerin leitet das Centrum für Translationale Medizin des Universitätsklinikums der Ruhr-Universität Bochum sowie die Arbeitsgruppe Transplantationsvirologie und Immunmonitoring an der Charité – Universitätsmedizin Berlin. Mit Ihrer Forschung will Babel dazu beitragen, die Wartezeiten auf Spendernieren zu verkürzen und die Lebensqualität der Menschen nach einer Transplantation zu verbessern. Da die Zahl der Betroffenen die Zahl der Spender weit übersteigt, liegt die Wartezeit für eine Niere in Deutschland zurzeit bei sieben bis acht Jahren.
Am ersten Samstag im Juni ist in ganz Deutschland der Tag der Organspende. Aufgrund der aktuellen Situation findet er in diesem Jahr ausschließlich online statt. Virtuelle Events und Aktionen auf der Homepage sowie den sozialen Netzwerken von Facebook, Instagram und YouTube werden den Tag der Organspende begleiten.
organspendetag.de
Das Ziel: Transplantierte Organe sollen länger leben
In dem vom Bundesministerium für Bildung und Forschung (BMBF) geförderten Projekt e:Kid entwickeln Babel und ihr Team neue Methoden, um die Funktionsdauer transplantierter Spendernieren zu verlängern. „Die mittlere Überlebenszeit der Transplantate liegt aktuell bei nur zehn Jahren“, so Babel. „Danach brauchen die Empfänger erneut ein Spenderorgan. Wenn wir also die Überlebenszeit der Transplantate verlängern, verkürzen wir damit zugleich Wartelisten und Wartezeiten.“
Dafür wollen die e:Kid-Forscherinnen und Forscher die Immunsuppression – die gezielte Unterdrückung des Immunsystems – nach einer Transplantation optimieren. Diese Therapie verhindert, dass das Immunsystem ein gespendetes Organ als „fremd“ erkennt, angreift und zerstört. Doch jede Immunsuppression ist eine Gratwanderung: „Zu wenig führt zu Funktionseinbußen des Spenderorgans bis hin zur Abstoßung. Zu viel Immunsuppression macht die Patientinnen und Patienten anfällig für Infektionen und andere ernsthafte Gesundheitsrisiken“, so Babel.
Ziel der Forschenden ist es, die gängige Standardtherapie durch ausbalancierte personalisierte Therapien zu ersetzen. „Jedes Immunsystem ist einzigartig. Die Organspende-Empfänger tragen daher ganz unterschiedlich hohe Risiken für immunologische Komplikationen. An dieses persönliche Risiko wollen wir die Immunsuppressionstherapie künftig in jedem Einzelfall anpassen – und dabei soll uns Künstliche Intelligenz helfen“, so Babel.
Künstliche Intelligenz für personalisierte Therapien
Zahlreiche Faktoren beeinflussen die Reaktionen des menschlichen Immunsystems und somit den Erfolg einer Transplantation. „Um besser zu verstehen, warum bestimmte Patientinnen und Patienten ein Jahr nach der Transplantation eine gut funktionierende Niere haben, andere aber nicht, haben wir den Verlauf der Transplantation von rund 600 Betroffenen erforscht. In mehr als 10.000 Proben haben wir die Komponenten des Immunsystems auf verschiedenen Ebenen – von den Genen bis zu den Proteinen – unter die Lupe genommen“, so Babel. Im nächsten Schritt spürten die Forschenden mit intelligenten Programmen in den molekularen und klinischen Daten spezifische Muster und Biomarker auf, die mit dem Erfolg einer Transplantation zusammenhängen. Auf dieser Grundlage entwickelten Babel und ihr Team zwei Computermodelle, die auf Künstlicher Intelligenz basieren. Mit dem einen Modell werden sie versuchen, bereits vor oder früh nach der Transplantation das Risiko einer Abstoßung individuell vorherzusagen. Ist das Risiko hoch, wird die Patientin oder der Patient mit einer stärkeren immunsuppressiven Therapie behandelt. Bei Erkrankten mit niedrigem Abstoßungsrisiko kann die immunsuppressive Therapie dagegen minimiert werden - somit können auch unerwünschte Nebenwirkungen der Medikamente vermindert werden. Durch das Training mit den pseudonymisierten Daten von 600 Patientinnen und Patienten lernten die intelligenten Programme, die Transplantationsrisiken mit einer Zuverlässigkeit von 80 Prozent vorherzusagen.
Erfolgsfaktor der Systemmedizin: Interdisziplinäre Zusammenarbeit
Der systemmedizinische Ansatz von e:Kid erfordert die Zusammenarbeit zahlreicher Fachbereiche: Transplantationsmedizin, Immunologie, Molekularbiologie, Biochemie, Physik, Datenwissenschaften und Bioinformatik. „Das ist ganz essenziell für den Erfolg unseres Projektes. Denn wir benötigen die Expertise der Klinik für die Interpretation der Ergebnisse, die Forschungsarbeit im Labor um die Daten zu generieren und IT-Expertinnen und Experten, um die riesigen Datenmengen auszuwerten und unsere Vorhersagewerkzeuge zu entwickeln“, betont Babel.
Die BMBF-Initiative „e:Med – Maßnahmen zur Etablierung der Systemmedizin“
Das Bundesministerium für Bildung und Forschung (BMBF) fördert e:Kid im Rahmen der e:Med-Initiative. Forscherinnen und Forscher analysieren dabei durch Laborexperimente gewonnene große Datenmengen mit innovativen IT-Lösungen, auch mit den Methoden der Künstlichen Intelligenz. Die Ergebnisse der Computeranalysen und -simulationen fließen wiederum in die Folgeexperimente ein. Dieses Wechselspiel von Experimenten und der Modellierung von Lebensprozessen im Computer charakterisiert die Systemmedizin. Ihr Ziel ist es, komplexe Prozesse in ihrer Gesamtheit zu erfassen, Vorhersagen zu ermöglichen und dadurch neue Ansatzpunkte für innovative Therapie- und Präventionsverfahren zu schaffen.
Ausblick
Aktuell überprüfen Babel und ihr Team den Mehrwert der Vorhersagemodelle an einhundert Patientinnen und Patienten. Nach der Nierentransplantation begleiten die e:Kid-Forscherinnen und -Forscher die Studienteilnehmenden für ein Jahr . Wenn sich dabei die bisherigen Ergebnisse bestätigen, könnte der Einsatz der Vorhersage-Tools für die personalisierte Immunsuppression in der Klinik etabliert werden und Ärztinnen und Ärzte künftig bei ihren therapeutischen Entscheidungen unterstützen. „Unsere Patientinnen und Patienten berichten immer wieder, dass sie die Zeit an der Dialyse als ‚verlorene Lebenszeit‘ empfinden. Wenn unsere Modelle helfen, die Lebensdauer der Organe zu verlängern und die Wartelisten zu verkürzen, bedeutet das für die Betroffen einen großen Gewinn an Lebensqualität“, so Babel. Zudem hofft sie, dass die Erkenntnisse der e:Kid-Studie auch auf die Transplantation anderer Organe übertragbar sind.
Die Zellen unseres Immunsystems können köpereigene von körperfremden Proteinen unterscheiden. So können sie Bakterien oder Viren aufspüren und bekämpfen. Aber auch lebensrettende Spenderorgane tragen körperfremde Proteine auf ihrer Oberfläche. Damit das Immunsystem sie nicht abstößt, prüfen Medizinerinnen und Mediziner vor jeder Transplantation, zu welchem Empfänger die Gewebemerkmale eines Spenderorgans besonders gut passen: Je besser die Merkmale von Spender und Empfänger übereinstimmen, desto geringer ist die Gefahr der Abstoßung.