Viele Menschen entwickeln aufgrund eines nicht optimalen Heilungsprozesses nach einem Infarkt eine Herzschwäche. Forschende aus Würzburg suchen nach körpereigenen Immunzellen, die neue Therapiemöglichkeiten eröffnen könnten.
Nach einem überstandenen Herzinfarkt entwickeln viele Menschen eine Herzschwäche; Würzburger Forschende suchen nach Biomarkern im Blut, die den Heilungsprozess am Herzen verbessern.
DLR Projektträger / BMBF
Der Herzinfarkt, eine der häufigsten Todesursachen weltweit, hinterlässt auch bei den Menschen, die ihn überstehen, bleibende Narben: Oft können sich die betroffenen Herzgefäße nicht wieder vollständig erholen, kann das erkrankte Herzgewebe nicht optimal ausheilen. Trotz guter Behandlungsmöglichkeiten des akuten Infarkts ist dieser Heilungsprozess in großen Teilen noch unverstanden und kann in einer permanenten Herzschwäche münden.
Hinweise auf neue Therapieoptionen könnten im menschlichen Immunsystem versteckt sein: Forschende des Deutschen Zentrums für Herzinsuffizienz (DZHI) am Universitätsklinikum Würzburg suchen nach Biomarkern im Blut, die die Heilung des vernarbten Gewebes unterstützen können. Das Forschungsprojekt mit dem Kürzel AIR-MI wird vom Bundesministerium für Bildung und Forschung (BMBF) mit knapp 300.000 Euro gefördert.
„Wir wissen, dass Herzinfarkte spezifische Immunreaktionen auslösen und dass die erworbene Immunabwehr hier eine entscheidende Rolle spielt“, erläutert Projektleiter Dr. Gustavo Ramos. „Bis heute gibt es jedoch keine etablierten Methoden, um die im Herzen ablaufenden Heilungsprozesse qualitativ zu bewerten. Wir können bislang also auch nicht sagen, wie, wann und bei welchen Betroffenen man eingreifen sollte, um wichtige Reparaturprozesse zu fördern.“
Im Fokus: Lymphozyten und T-Zell-Rezeptoren
Ganz gezielt nehmen die Wissenschaftlerinnen und Wissenschaftler um Ramos deshalb die T-Lymphozyten unter die Lupe – weiße Blutkörperchen, die einen Teil des adaptiven Immunsystems ausmachen (s. Kasten). Eine umfassende, parallel stattfindende Sequenzierung von T-Zell-Rezeptoren soll helfen, das spezifische Profil von Immunzellen zu beschreiben, die eine aufbauende Therapie positiv beeinflussen könnten. „Diese Methode der Sequenzierung ist zwar nicht neu, in der Anwendung auf eine im Vorfeld sehr gut charakterisierte Patientengruppe aber einzigartig. Sie stellt damit einen innovativen und sehr unvoreingenommenen Forschungsansatz dar“, so Ramos. Die gewonnenen Erkenntnisse will die Forschungsgruppe im Mausmodell und in funktionellen Studien direkt miteinander vergleichen.
In ihren Untersuchungen setzen die Forschenden auf die enge Zusammenarbeit mit internationalen Forschungseinrichtungen. Das Projekt beruht auf einem multinationalen Konsortium im Rahmen des Europäisches Netzwerks zu Herz-Kreislauf-Erkrankungen (ERA-CVD). Ramos arbeitet mit Prof. Dr. Peter Rainer von der Medizinischen Universität Graz, Österreich, und Prof. Maria Encarnita Mariotti-Ferrandiz von der Universität Sorbonne, Frankreich, eng zusammen. Ohne die Zusammenführung der jeweiligen Expertise wäre das Projekt nicht möglich, betont der Wissenschaftler.
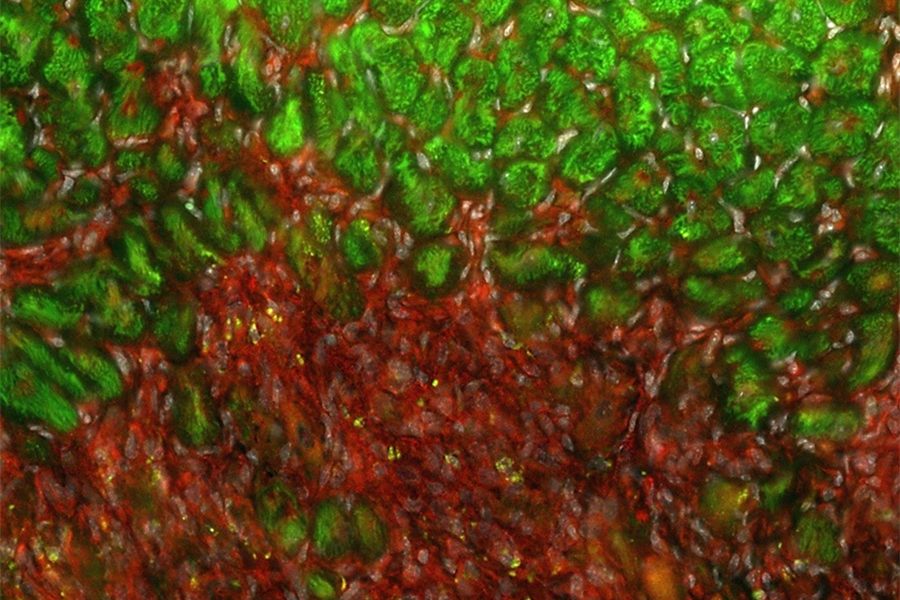
Mikroskopische Aufnahme von Herzgewebe nach einem Infarkt mit einem nicht optimalen Heilungsprozess. Die Aufnahme zeigt funktionsfähige Herzmuskelzellen (grün) sowie durch den Infarkt entstandenes Narbengewebe (rot).
G. Ramos
Hoffnung auch im Kampf gegen Covid-19
Die Konsortiumsmitglieder in Graz, Würzburg und Paris werden deshalb in einem im Rahmen des Forschungsvorhabens neu entstandenen Projektes auch untersuchen, welche Rolle die T-Zellen bei einer Schädigung des Herzmuskels durch das SARS-CoV-2 Virus spielen. Dass das Virus Herzschäden verursachen kann, ist erwiesen, die genauen Mechanismen dafür sind allerdings noch unbekannt. Belegt ist zudem, dass auch Monate nach einer Infektion mit dem SARS-CoV-2-Virus immer noch entsprechende T-Zellen existieren. Das internationale Forschungsteam erhofft sich, durch die Arbeiten ein besseres Verständnis der kardialen Immunantwort bei Covid-19 -Patientinnen und Patienten zu gewinnen.
Der Herzinfarkt zählt zu den häufigsten Todesursachen in den Industrieländern; er entsteht durch einen plötzlichen Verschluss von Blutgefäßen des Herzmuskels bzw. der Herzkranzgefäße. Weil der Herzmuskel damit von der Sauerstoffversorgung abgeschnitten ist, kann er seine Arbeit nicht mehr verrichten. Typische Anzeichen für einen Infarkt sind plötzlich auftretende, starke Schmerzen in Brust und Rücken, starke Beklemmungsgefühle und Atemnot. Frauen weisen darüber hinaus häufig andere Symptome auf, beispielsweise Kurzatmigkeit, Übelkeit, Kiefer- und Halsschmerzen sowie Beschwerden im Oberbauch. Aber: Nicht alle Menschen haben diese typischen Symptome. Um einen Herzinfarkt so gut wie möglich behandeln zu können, gilt es die Anzeichen dieser lebensbedrohlichen Erkrankung möglichst früh zu erkennen.
Wie das Immungedächtnis Erreger in Schach halten kann
Auf fremde Organismen oder Substanzen reagiert der menschliche Körper mit einer Immunantwort. Man unterscheidet zwischen einer angeborenen und einer erworbenen (oder auch adaptiven) Reaktion des Immunsystems. Bei letzterer kann das Immunsystem flexibel auf fremde Reize reagieren. Insbesondere die sogenannten T-Zellen – weiße Blutkörperchen, die einen Teil des adaptiven Immunsystems ausmachen – stellen eine wichtige Säule der Immunabwehr dar. Manche dieser T-Zellen, die T-Gedächtniszellen, können sich auch noch Jahre nach einer Infektion an einen bestimmten Erreger „erinnern“ und die Immunreaktion entsprechend schnell ankurbeln. In der aktuellen Corona-Pandemie rücken die T-Zellen deshalb in den besonderen Fokus von Forscherinnen und Forschern.