Ein interdisziplinäres Forschungsteam entwickelt ein Modell, das die Interaktionen zwischen Immunzellen und dem umliegenden Gewebe abbildet. Das ist nicht nur für die Krebsforschung, sondern auch für die Transplantationsmedizin von großer Bedeutung.
Um eine Krebserkrankung wirkungsvoll behandeln zu können, ist es wichtig, möglichst viel über die Tumore zu wissen. Gewebebiopsien spielen hierbei eine zentrale Rolle. Die mit einer feinen Nadel entnommenen Gewebeproben werden mikroskopisch untersucht und molekularpathologisch aufgearbeitet. Dadurch gewinnen die Medizinerinnen und Mediziner wichtige Informationen über den Tumor und den möglichen Krankheitsverlauf. „Die Biopsie stellt aber immer nur eine Momentaufnahme dar. Sie spiegelt das Geschehen zum Zeitpunkt der Gewebeentnahme wider“, sagt Professor Dr. Friedrich Feuerhake vom Institut für Pathologie der Medizinischen Hochschule Hannover. „Die Prozesse im Körper sind sehr dynamisch und beeinflussen sich wechselseitig. Das wirkt sich auch auf den Krankheitsverlauf aus. Die bislang etablierte Auswertung der Biopsien kann diese Dynamik nur zum Teil abbilden.“ Feuerhake leitet das Forschungsprojekt SYSIMIT, das zum Ziel hat, mehr prognostische Informationen aus den Gewebebiopsien zu gewinnen, um so zu einem besseren Krankheitsverständnis beizutragen. Dafür will das Konsortium diese Momentaufnahmen in einen krankheitsübergreifenden und dynamischen Kontext einordnen. Um dieses Ziel zu erreichen, arbeiten die Wissenschaftlerinnen und Wissenschaftler an einem mathematischen Modell, das die Prozesse im Gewebe simuliert – mithilfe neuer Methoden aus den Computerwissenschaften, der Bildanalyse, der Medizin, der Biologie und der Mathematik.
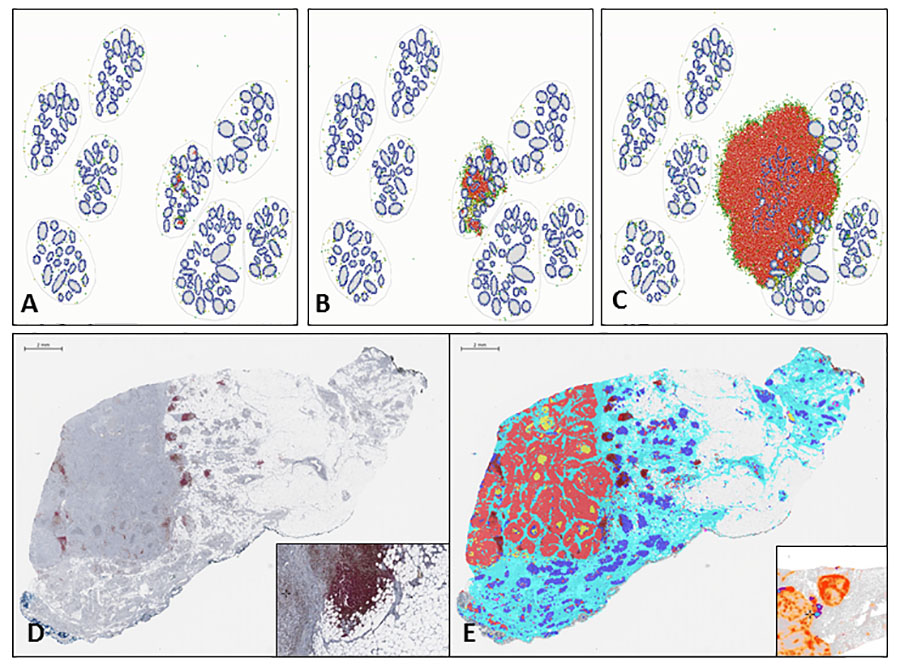
Die grafisch dargestellten Ergebnisse der Modellierung (A–C) zeigen, wie Immunzellen (grün/gelb) zunächst mit gesundem Brustdrüsengewebe (blau) und im Lauf des Tumorwachstums mit den Krebszellen (rot) interagieren. Die Resultate von Computersimulationen werden dann mit den Mustern der Immunzellinfiltrate in echten Biopsien (D) verglichen und quantitativ mit modernen Methoden der Bildanalyse (E) analysiert, um so das Stadium der Erkrankung sowie mögliche Therapieformen zu bestimmen.
Dr. J. C. Alfonso Lopez, Dr. Haralampos Hatzikirou,Dr. R. Schönmeyer, Prof. F. Feuerhake
Präzisere Therapien für die Krebsmedizin
Eine wichtige Rolle bei diesen dynamischen Prozessen spielt das Immunsystem. Bei Krebserkrankungen entstehen für Tumorzellen charakteristische Proteine, die vom Immunsystem als körperfremd erkannt werden können. Ein vielversprechender Ansatz im Kampf gegen Krebs ist es, diesen körpereigenen Abwehrmechanismus gezielt zu beeinflussen. Der medizinische Bereich, der sich mit diesem Ansatz beschäftigt – die Immuno-Onkologie –, konnte in den vergangenen Jahren enorme Fortschritte erzielen.
Das interdisziplinäre SYSIMIT-Team kombiniert die herkömmliche Mikroskopie mit mathematischen Modellierungen und innovativer Bildanalyse, um die Interaktionen zwischen Immun- und Krebszellen abbilden zu können. So konnten die Forscherinnen und Forscher bereits nachweisen, dass wechselnde hormonelle Einflüsse sich nicht nur auf das Drüsengewebe in der weiblichen Brust auswirken, sondern zugleich mit zyklischen Veränderungen des lokalen Immungeschehens einhergehen. Mit ihrem mathematischen Modell können die Forschenden den Einfluss von hormonellen Schwankungen auf das Gewebe und die Immunantwort des Körpers auf krebsinduzierende Zellschädigung simulieren. Inzwischen entwickeln die Wissenschaftlerinnen und Wissenschaftler ihr Modell weiter, um zukünftig auch fortgeschrittene Tumorstadien und die Wirkmechanismen von Medikamenten darstellen zu können. „So könnten wir in Zukunft dazu beitragen, neue Therapieansätze, die das Immunsystem zielgerichtet beeinflussen, sicherer, wirksamer und kosteneffizienter einzusetzen“, erläutert Feuerhake.
Überlebenszeit von Spendernieren erhöhen
Die Wissenschaftlerinnen und Wissenschaftler beschäftigen sich zudem mit weiteren Krankheitsprozessen, bei denen Wechselwirkungen zwischen Immunzellen und deren Zielstrukturen eine zentrale Rolle spielen. Mithilfe ihrer Simulationen wollen sie beispielsweise die Behandlung nach einer Nierentransplantation verbessern. Denn auch hier ist das Immunsystem von zentraler Bedeutung: Es erkennt Zellen der transplantierten Nieren als fremd und leitet eine entsprechende immunologische Reaktion ein. Damit diese beherrschbar bleibt und nicht zu einer Abstoßung des transplantierten Organs führt, müssen die Transplantationsempfänger zumeist lebenslang Medikamente einnehmen, die das Immunsystem unterdrücken. Eine solche Behandlung ist jedoch ein schwieriger Balanceakt, denn neben der erwünschten Reduzierung der Abstoßungsprozesse erhöht sie die Gefahr, dass der Körper bestimmte Infektionen nicht mehr so erfolgreich bekämpfen kann wie vor der Transplantation.
Auch hier liefern Gewebebiopsien wichtige Erkenntnisse, um die medikamentöse Therapie anzupassen und möglichst schnell auf akute Komplikationen zu reagieren. „Aus Sicht der digitalen Pathologie macht es für uns keinen großen Unterschied, ob wir die Interaktion von Immunzellen mit Krebszellen, mit gesundem Gewebe oder mit Zellen aus einer transplantierten Niere analysieren“, so Feuerhake. „Unser Ansatz, räumliche Informationen aus mikroskopischen Bildern in mathematische Modelle dynamischer Krankheitsprozesse zu integrieren, kann für verschiedene Organsysteme und Krankheitsprozesse wichtige Informationen liefern.“ Im Fall der Nierentransplantation dient die Forschung des Teams aus Hannover dem Ziel, dass Spenderorgane so lange wie möglich funktionstüchtig bleiben. Das hilft nicht nur den betroffenen Patientinnen und Patienten, sondern trägt auch dazu bei, den Bedarf an Spendernieren zu verringern.
Systemmedizin in Deutschland etablieren
Das Bundesministerium für Bildung und Forschung (BMBF) unterstützt das SYSIMIT-Konsortium im Rahmen des Förderkonzeptes „e:Med – Maßnahmen zur Etablierung der Systemmedizin in Deutschland“. Ziel der Systemmedizin ist es, neue Einsichten in die Prozesse des Lebens anzuwenden, um Krankheiten genauer zu diagnostizieren und besser zu behandeln. Denn ob ein Mensch gesund oder krank ist, hängt von vielen Faktoren ab, unter anderem von genetischen Unterschieden oder Umwelteinflüssen. Die Frage ist, wie all diese Faktoren und Systeme ineinandergreifen und wie sie zu beeinflussen sind. Um diese Frage zu beantworten, verwendet die Systemmedizin Methoden der mathematischen Modellierung und die Rechenkapazitäten modernster Hochleistungscomputer.
Originalpublikationen:
Schaadt, N. S., Schönmeyer, R., Forestier, G., et al. Graph-based description of tertiary lymphoid organs at single-cell level. PLoS Comput Biol. 2020 Feb 21;16(2): e1007385. doi: 10.1371/journal.pcbi.1007385.
Schaadt, N. S., Alfonso, J. C. L., Schönmeyer, R., et al. Image analysis of immune cell patterns in the human mammary gland during the menstrual cycle refines lymphocytic lobulitis. Breast Cancer Res Treat. 2017 Jul;164(2): 305-315. doi: 10.1007/s10549-017-4239-z.
Alfonso, J. C., Schaadt, N. S., Schönmeyer, R., Brieu, N., et al. In-silico insights on the prognostic potential of immune cell infiltration patterns in the breast lobular epithelium. Sci Rep. 2016 Sep 23;6:33322. doi: 10.1038/srep33322.
Ansprechpartner:
Prof. Dr. Friedrich Feuerhake
Institut für Pathologie
Medizinische Hochschule Hannover
Carl-Neuberg-Straße 1
30625 Hannover
feuerhake.friedrich@mh-hannover.de