Krebs beginnt meist schmerzfrei und unsichtbar: Eine der etwa 100 Billionen Zellen des menschlichen Körpers verliert die Kontrolle über ihr Wachstum und beginnt, sich unaufhörlich zu teilen. Ursache ist meist eine Mutation in den Erbanlagen der Zelle, die zufällig auftreten, durch Umwelteinflüsse entstehen oder vererbt sein kann. Welche genetischen Veränderungen den häufigsten Krebserkrankungen zugrunde liegen, möchten Wissenschaftlerinnen und Wissenschaftler aus der ganzen Welt im Internationalen Krebsgenom-Konsortium, kurz ICGC, verstehen. (Newsletter 62 / April 2013)
 Dr. Ursula Weber, Projektmanagerin des PedBrainTumor-Projektes am Deutschen Krebsforschungszentrum HeidelbergAuch Deutschland ist beteiligt – ein Projekt untersucht die Ursachen kindlicher Hirntumore. Dr. Ursula Weber vom Deutschen Krebsforschungszentrum in Heidelberg erklärt im Interview, welche Ziele verfolgt werden und welche ersten Ergebnisse es gibt.
Dr. Ursula Weber, Projektmanagerin des PedBrainTumor-Projektes am Deutschen Krebsforschungszentrum HeidelbergAuch Deutschland ist beteiligt – ein Projekt untersucht die Ursachen kindlicher Hirntumore. Dr. Ursula Weber vom Deutschen Krebsforschungszentrum in Heidelberg erklärt im Interview, welche Ziele verfolgt werden und welche ersten Ergebnisse es gibt.
Frau Dr. Weber, Sie untersuchen die genetischen Ursachen von Hirntumoren bei Kindern. Warum ist das sinnvoll?
Krebs ist nicht gleich Krebs und von Patient zu Patient können sich auch Tumoren derselben Organe stark unterscheiden. Das gilt auch für Hirntumoren bei Kindern. Selbst bei Krebserkrankungen, in denen sich die Tumorzellen unter dem Mikroskop scheinbar nicht unterscheiden, sprechen manche Patienten sehr gut auf bestimmte Therapien an, andere Patienten hingegen nicht. Das deutet darauf hin, dass oftmals die Ausbreitung und Entwicklung einer Krebserkrankung ganz individuell von der genetischen Ausstattung des Tumors abhängig sind. Deshalb ist es wichtig, die Tumore genetisch exakt zu charakterisieren.
Was untersuchen Sie genau?
Ziel des PedBrainTumor-Projektes ist es, 500 Gewebeproben kindlicher Hirntumoren mit neusten Sequenziermethoden zu entschlüsseln. Dabei nutzen wir das sogenannte „Next-Generation Sequencing“, oder auch Hochdurchsatz-Sequenzierung genannt, bei der ein ganzes menschliches Genom innerhalb von zwei Wochen komplett sequenziert, also entschlüsselt, werden kann. Im Projekt geht es darum, sowohl alle Mutationen, also Veränderungen im Erbgut, zu erfassen, als auch alle Veränderungen in der Aktivität von Genen und in epigenetischen Informationen. Letztere steuern den Gebrauch der DNA und bestimmen, welche Gene wann und wo genau an- oder abgeschaltet werden. Gleichzeitig untersuchen wir auch 500 Proben von gesundem Gewebe der Tumorpatienten, um ganz genau abgleichen zu können, welche genetischen Veränderungen für den Tumor einzigartig sind. Die Gesamtheit dieser Informationen soll dazu beitragen, grundlegende Erkenntnisse über die Entstehung pädiatrischer Hirntumoren zu erhalten, die Tumorbiologie besser zu verstehen und letztlich auf Grundlage dieser Kenntnis neue zielgerichtete Therapien zu entwickeln.
Neue Therapien sind vermutlich gerade für kindliche Hirntumoren dringend erforderlich?
Ja, besonders dringend brauchen wir neue, zielgerichtete und schonende Therapieverfahren. Die pädiatrischen Hirntumoren sind die häufigste Krebserkrankung im Kindesalter, die einen tödlichen Verlauf hat. Die Behandlung der Tumoren und die damit verbundenen Nebenwirkungen sind oft sehr belastend für die Kinder und können das heranwachsende Gehirn in seiner Entwicklung beeinträchtigen. Wir beschränken uns in unseren Untersuchungen auf die beiden häufigsten kindlichen Hirntumoren, das Medulloblastom und das pilozytische Astrozytom. In Deutschland sind jedes Jahr etwa 300 Kinder von diesen Hirntumoren betroffen.
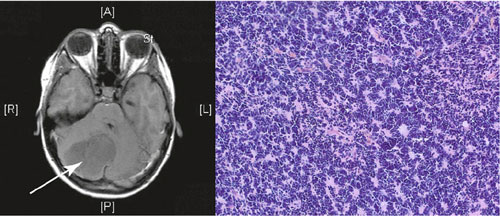
Magnetresonanztomografie (links, der Pfeil deutet auf den Tumor) und Gewebeschnitt
(rechts) eines Medulloblastoms
Was könnte die Entschlüsselung der Tumorgenome zu einer verbesserten Therapie beitragen?
Genetische Veränderungen können zum Beispiel Hinweise auf die Ursache der Tumore geben und als Zielstrukturen für neue personalisierte Therapieansätze dienen. Gleichzeitig geht es uns darum, die Tumoren anhand ihrer Genetik in Untergruppen einzuteilen. So sollen zukünftig ganz genau die Patienten identifiziert werden, die von einer bestimmten Therapie, zum Beispiel einer Chemotherapie, profitieren. Denn wie ich eingangs gesagt habe, sind viele Tumoren unter dem Mikroskop nicht zu unterscheiden. Genetisch jedoch unterscheiden sie sich erheblich. Und davon kann auch die Wahl der Therapie abhängen.
Haben Sie bereits Ergebnisse erzielen können?
Die Sequenzierung von 125 Medulloblastomen hat bereits zu einer deutlich verbesserten Einteilung der Tumoren in Untergruppen beigetragen, als es bisher möglich war. Ein interessantes Ergebnis ist, dass kindliche Medulloblastome – obwohl es sich um hochaggressive Tumoren handelt – deutlich weniger Mutationen tragen als alle Tumoren von Erwachsenen, die bislang untersucht wurden. Eine häufige Mutation, die wir bei einem anderen pädiatrischen Hirntumor, dem Glioblastom, gefunden haben, liegt in einem Gen, das für die Verpackung der DNA verantwortlich ist und so auch die Aktivität von Genen bestimmt. Genauer handelt es sich um das Gen Histonmodifikation H3.3. Somit ist klar: In kindlichen Hirntumoren sind auch epigenetische Faktoren, die den Gebrauch der DNA steuern, durch Mutation verändert.
Wie geht es jetzt weiter?
In den nächsten Jahren werden wir wie geplant die übrigen 250 Tumorproben und noch mal so viele Kontrollen analysieren. Wir werden neue Befunde validieren und häufig gefundene spezielle Veränderungen in Tiermodelle übertragen, um die präklinische Testung neuer klinischer Therapien durchzuführen. Alle gesammelten Daten werden in einer großen Datenbank im Rahmen des Internationalen Krebsgenom- Konsortiums zusammengefasst und der internationalen Forschungsgemeinschaft zur Verfügung gestellt.
Kürzlich erhielt ein Wissenschaftler des ICGC den Deutschen Krebspreis.
Genau. Der Heidelberger Molekularbiologe und Kinderarzt Professor Dr. Stefan Pfister wurde für seine Untersuchungen zu den molekularen Eigenschaften bösartiger Hirntumoren bei Kindern ausgezeichnet. Mit diesem Preis hat die Deutsche Krebsgesellschaft seine Verdienste in der translationalen Krebsforschung gewürdigt. Bei translationaler Forschung in der Medizin geht es um die frühzeitige Übertragung von grundlegenden Forschungserkenntnissen in die therapeutische Anwendung.